Benefici, rischi e indicazioni per la somministrazione del vaccino di Oxford dopo l’ultimo parere dell’Ema
Rimangono ancora molto dubbi intorno ad AstraZeneca. Il vaccino anti-Covid doveva essere per l’Italia la via d’uscita dalla pandemia ma neanche il tentativo dell’Agenzia europea dei medicinali è riuscito a fare chiarezza. Ecco tutto quello che sappiamo sul vaccino fino ad ora.
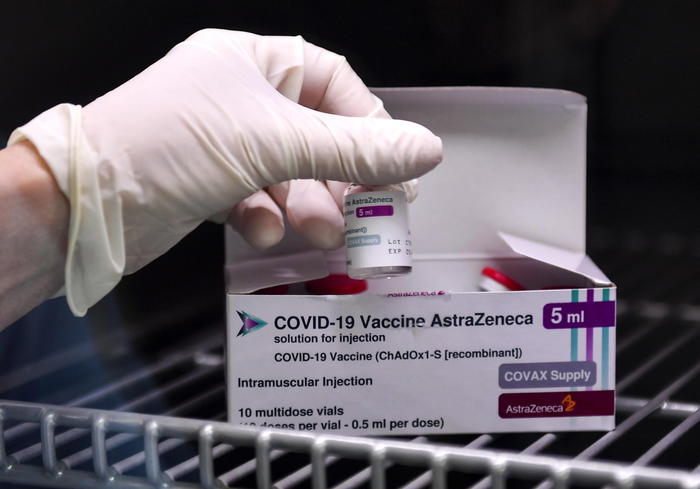
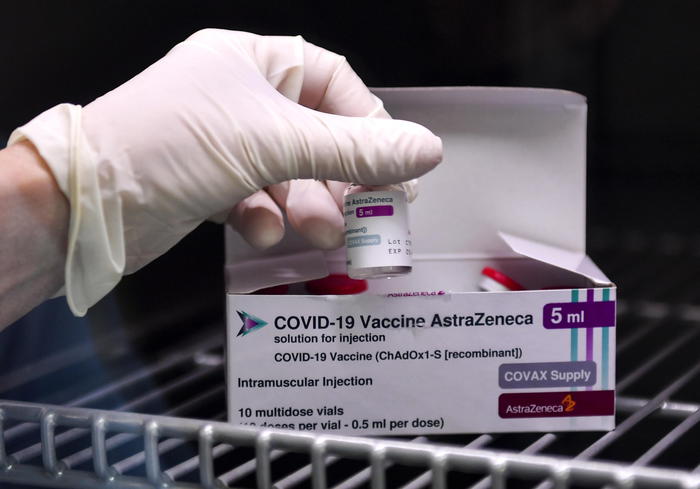
AstraZeneca, ribattezzato Vaxzevria lo scorso 25 marzo, è nato da una ricerca che ha coinvolto lo Jenner Institute dell’Università di Oxford e la sua società spin-out, Vaccitech, in collaborazione con la società anglosvedese AstraZeneca e l’italiana IRBM Science Park.
Il vaccino usa un vettore virale basato su una versione indebolita del comune virus del raffreddore (adenovirus). Questo contiene il “materiale genetico” che codifica per la proteina Spike del virus SARS-CoV-2. In questo modo, con la somministrazione del vaccino nel soggetto sano, la proteina spike superficiale viene prodotta dall’organismo, stimolando il sistema immunitario ad attaccare il virus SARS-CoV-2 in caso di infezione.
Il vaccino AstraZeneca è entrato nell’ultima fase di sperimentazione lo scorso dicembre e il 30 dello stesso mese è stato approvato per l’uso nel programma di vaccinazione del Regno Unito. La prima dose è stata somministrata il 4 gennaio 2021. Il 12 gennaio 2021 l’Ema ha ricevuto la domanda di autorizzazione condizionata all’immissione in commercio da AstraZeneca, il parere positivo dell’Agenzia è arrivato il 29 gennaio.
Gli studi sull’efficacia di AstraZeneca hanno dimostrato un’incidenza del 62,2% nello sviluppo di anticorpi neutralizzanti contro il virus negli individui vaccinati, percentuale che aumenta in caso di sviluppo di forme gravi della malattia.
Secondo quanto affermato dalla direttrice generale alla Salute della Commissione Europea Sandra Gallina, in audizione alla commissione Bilancio del Parlamento Europeo a Bruxelles, l’Ue paga ad AstraZeneca per ogni dose di vaccino anti Covid più di 1,78 euro. La cifra è emersa a dicembre, quando l’europarlamentare belga Eva De Bleeker ha erroneamente reso pubblici i prezzi delle singole dosi, ancora coperti da segreto.
Nella giornata di ieri, dopo i vari stop alla somministrazione nei vari Paesi europei, l’Ema ha pubblicato un nuovo rapporto. In questo è stato riconosciuto un forte legame tra la somministrazione del vaccino anti-Covid di AstraZeneca e alcuni casi estremamente rari di eventi trombotici cerebrali e addominali, associati a carenza di piastrine nel sangue. Per la redazione del rapporto, l’Agenzia ha analizzato 62 casi di trombosi cerebrale dei seni venosi e 24 casi di trombosi addominali, segnalati fino al 22 marzo 2021. Di questi casi, 18 hanno avuto decorso letale. I numeri di confronto vedono, dall’altra parte, 25 milioni di persone vaccinate nello Spazio economico europeo e nel Regno Unito. Il totale dei casi riportati fino al 4 aprile sono stati 169 riguardo alle trombosi cerebrali e 53 per le trombosi addominali, su 34 milioni di persone vaccinate.
L’Ema ha dunque concluso che queste trombosi combinate con bassi livelli piastrinici dovrebbero essere elencate fra i possibili effetti collaterali, molto rari, del farmaco di AstraZeneca. Contestualmente, l’Agenzia ha sottolineato che il rischio di mortalità del virus è di gran lunga maggiore dei possibili effetti avversi del vaccino. Il responso finale è che il giudizio sul rapporto rischi-benefici del vaccino e sulla sua efficacia contro il coronavirus SARS-CoV-2 è nettamente positivo.
Sebbene non sia ancora stato individuato un fattore di rischio specifico, al momento la casistica in Europa riguarda soprattutto le donne sotto i 55-60 anni, entro un intervallo di due settimane dalla somministrazione del vaccino. A tal proposito, l’Ema ha specificato che non c’è modo di indicare che i contraccettivi o la gravidanza siano un fattore di rischio per i casi osservati. Lo stesso discorso vale per l’indicazione precisa di sesso, età e patologie preesistenti. Non è possibile quindi raccomandare la limitazione delle somministrazioni a gruppi specifici.
Il 7 aprile l’Ema ha inoltre sottolineato che casi analoghi di trombosi sono stati segnalati anche dopo la somministrazione di altri vaccini autorizzati nell’Unione europea, oltre a quelli di AstraZeneca. In particolare sarebbero 35 casi per il vaccino Comirnaty di Pfizer-BioNTech, su 54 milioni di persone vaccinate nello Spazio economico europeo; 5 casi per il vaccino di Moderna su 4 milioni di persone vaccinate nel mondo; e per quanto riguarda Johnson & Johnson (che è l’unico degli altri vaccini oggi disponibili nell’Ue a utilizzare un vettore virale come quello di AstraZeneca) ci sono 3 casi su 4,5 milioni di persone vaccinate nel mondo.
Per il momento è consigliato ai pazienti che hanno ricevuto le dosi del vaccino AstraZeneca il monitoraggio di possibili sintomi anomali come respiro corto, dolore al petto, gonfiore alle gambe, dolore addominale persistente, sintomi neurologici come forti emicranie o vista sfocata, macchie di sangue sottocutanee nel sito dell’iniezione. Nell’eventualità in cui questi si presentino si raccomanda l’immediata richiesta di assistenza medica.
In merito alla discussione sui possibili trattamenti, l’Ema fa sapere che gli operatori sanitari non devono usare l’eparina se sospettano di trovarsi di fronte a uno di questi casi. Sull’uso di altri anticoagulanti i pareri scientifici sono discordanti. Altri possibili trattamenti includono immunoglobuline, steroidi e plasmaferesi.
In risposta al rapporto dell’Agenzia, Germania, Spagna e Belgio hanno deciso l’uso sopra i 60 anni, la Francia sopra i 55. La Gran Bretagna ha raccomandato di offrire un vaccino diverso alle persone con meno di 30 anni. Gli Stati Uniti, invece, ha fatto sapere Anthony Fauci, non prevedono al momento di utilizzare il vaccino di Oxford.
Per quanto riguarda l’Italia, la nuova circolare del ministero della Salute ha ribadito che il vaccino Vaxzevria di AstraZeneca è approvato dai 18 anni d’età. «Sulla base delle attuali evidenze, tenuto conto del basso rischio di reazioni avverse di tipo tromboembolico a fronte dell’elevata mortalità da Covid nelle fasce di età più avanzate» – si legge – «si rappresenta che è raccomandato un suo uso preferenziale nelle persone sopra i 60 anni».
In merito alla seconda dose per chi ha già ricevuto la prima, l’orientamento dell’Aifa è quello di far concludere l’immunizzazione con AstraZeneca a chi ha fatto la prima dose non essendo stato segnalato alcun caso di trombosi dopo la somministrazione della seconda dose.
di: Alessia MALCAUS
FOTO: EPA/GEORGI LICOVSKI
Ti potrebbe interessare anche: