Le autorità americano vogliono analizzare i rischi legati alla miocardite. Possibile che l’analisi sia completata non prima di gennaio 2022
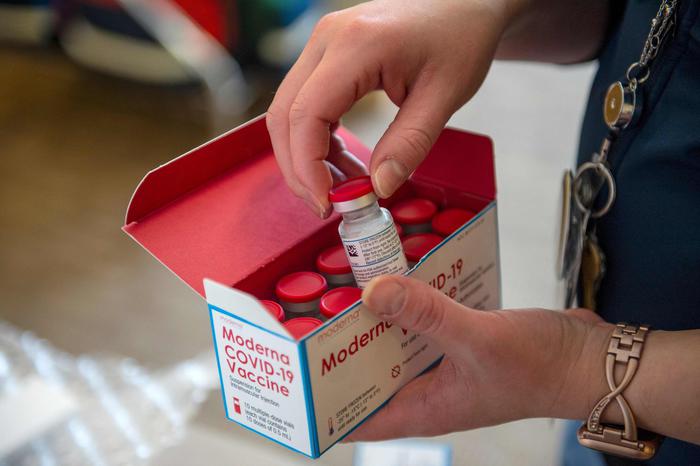
Brutte notizie per Moderna. La Food and Drug Administration statunitense ha rinviato la propria decisione sull’autorizzazione del suo vaccino negli adolescenti di età compresa tra i 12 ed i 17 anni. Lo ha reso noto la stessa società, precisando di aver ricevuto una comunicazione dall’agenzia nella quale la informava che l’analisi potrebbe essere completata non prima di gennaio del prossimo anno.
Moderna aveva richiesto l’autorizzazione della FDA per l’uso negli adolescenti a giugno. Il motivo di questo ritardo è legato alla necessità di analizzare i rischi legati a un raro effetto collaterale: la miocardite, infiammazione cardiaca che ha interessato principalmente giovani di sesso maschile dopo la seconda dose.
«La sicurezza dei destinatari del vaccino è di fondamentale importanza per Moderna. La Società è pienamente impegnata a lavorare a stretto contatto con la FDA per supportare la loro revisione ed è grata alla FDA per la loro diligenza», ha affermato Moderna in una nota, informando anche che ritarderà la presentazione della richiesta per i bambini di età compresa tra 6 e 11 anni.
di: Maria Lucia PANUCCI
FOTO: Joseph Prezioso / AFP
Ti potrebbe interessare anche: