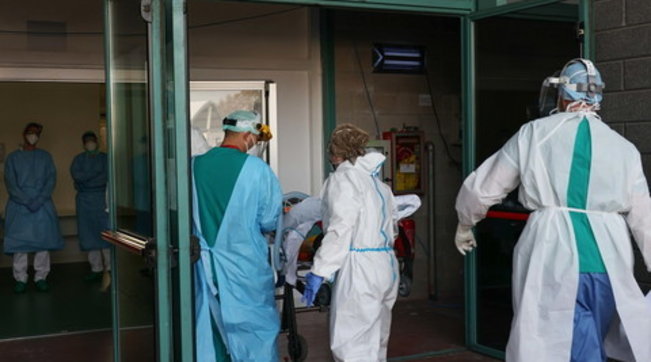
Il Brasile ha sospeso invece i test del vaccino cinese Sinovac
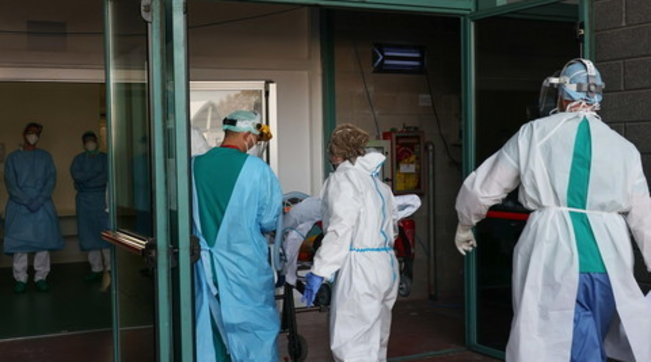
Continuano le buone notizie sul fronte della lotta al Covid-19. Dopo l’annuncio di Pfizer e Biontech sull’efficacia al 90% del loro vaccino anti-Covid in fase 3, l’ultima prima dell’eventuale approvazione (leggi qui). ora la big statunitense Eli Lilly ha ottenuto dalla Fda l’agenzia sanitaria Usa, il via libera d’urgenza all’uso del trattamento anti-Covid a base di anticorpi monoclonali per curare infezioni di limitata entità in adulti e bambini.
Il trattamento, denominato bamlanivimab (LY-CoV555), è infatti da applicare ai casi di Covid da lieve a moderato, quindi alle persone recentemente infettate, non anche ai pazienti ospedalizzati. La cura va somministrata il prima possibile ad adulti e pazienti pediatrici oltre i 12 anni, subito dopo il test positivo ed entro 10 giorni dalla comparsa dei sintomi nelle strutture ospedaliere o in altre strutture sanitarie.
La cura di Eli Lilly è a base di anticorpi monoclonali, ovvero proteine prodotte in laboratorio che riproducono il funzionamento del sistema immunitario nel combattere i virus. In questo caso il bamlanivimab è un anticorpo monoclonale specificamente diretto contro la proteina spike di SARS-CoV-2 e consente di bloccare l’aggressione del virus. E’ il primo trattamento a base di anticorpi monoclonali che riceve l’autorizzazione.
Notizie non confortanti arrivano invece dal Brasile che ha reso noto di aver sospeso le sperimentazioni del vaccino contro il Covid-19 prodotto dalla cinese Sinovac a causa di un “grave incidente” che ha coinvolto un volontario, avvenuto lo scorso 29 ottobre. Lo ha annunciato l’ente regolatore brasiliano che però non ha fornito dettagli in merito all’accaduto.
Un duro colpo dato che il vaccino avrebbe dovuto essere distribuito entro il 20 novembre in Brasile che ne aveva già acquistate 120 mila dosi.
di: Maria Lucia PANUCCI
FOTO: ANSA
Ti potrebbe interessare anche: